-
Câu Hỏi
1868
-
Thành Viên
799
-
Wiki-Hỏi-Đáp.Org
Wiki Hỏi đáp trực tuyến là website chia sẻ kiến thức cộng đồng về tất cả lĩnh vực từ giáo dục, kinh tế, xã hội khoa học, đời sống, gia đình...
Liên hệ tại: Wikihoidap.org@gmail.com
Liên kết hữu ích bạn nên xem: Alo789
-
Theo dõi Wiki Hỏi đáp
-
Bản quyền tại DMCA
Benzen là gì? Tổng hợp kiến thức benzen hóa 9 và Các dạng bài tập
Chương trình hóa phổ thông, các chất hóa học hữu cơ dạng vòng thơm đặc biệt được chú trọng, nhất là benzen. Đây là kiến thức nền tảng nhằm học lên cao các kiến thức khác. Vậy hãy cùng Wikihoidap.org tìm hiểu kỹ hơn về các tính chất, đặc điểm của benzen nhé!
Danh mục nội dung
Benzen là gì?
Benzen là một hợp chất hữu cơ có công thức hóa học C6H6. Benzen là một hidrocacbon thơm, trong điều kiện bình thường là một chất lỏng không màu, mùi dịu ngọt dễ chịu, dễ cháy. Benzen tan rất kém trong nước và rượu. Vì chỉ chứa carbon và hydro nên benzene là một hydrocarbon.
Tính chất vật lý của Benzen
Benzen là chất lỏng, không màu, không tan trong nước, nhẹ hơn nước, hòa tan nhiều chất hữu cơ như: dầu ăn, nến, cao su, iot....
Benzen độc, cần cẩn thận làm thí nghiệm và sử dụng.
Tính chất hóa học của Benzen
1. Phản ứng thế
a) Thế nguyên tử H của vòng benzen
* Phản ứng với halogen
- Cho benzen và brom vào ống nghiệm khô rồi lắc nhẹ hỗn hợp.
- Cho tiếp một ít bột sắt vào ống nghiệm trên, lắc nhẹ. Màu của brom nhạt dần và thấy có khí hiđro bromua thoát ra do đã xảy ra phản ứng thế:
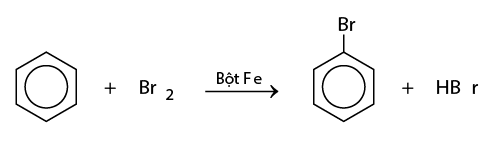
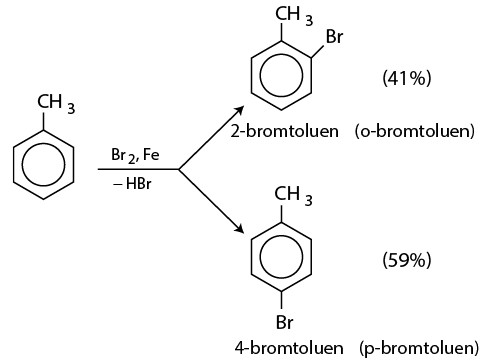
- Nếu cho các ankylbenzen phản ứng với brom trong điều kiện có bột sắt sẽ thu được hỗn hợp sản phẩm thế brom chủ yếu vào vị trí para và ortho so với nhóm ankyl:
* Phản ứng với axit nitric
- Cho benzen vào ống nghiệm chứa sẵn hỗn hợp H2SO4 đặc và HNO3 đặc. Khi đó sẽ thấy có lớp chất lỏng nặng màu vàng nhạt lắng xuống. Đó là nitrobenzen được tạo thành theo phản ứng:
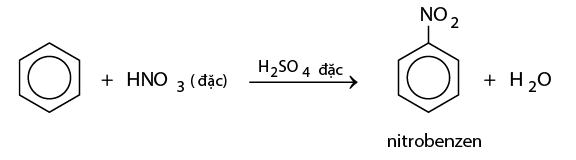
- Toluen tham gia phản ứng nitro hóa dễ dàng hơn benzen (chỉ cần HNO3 đặc, không cần HNO3 bốc khói) tạo thành sản phẩm thế vào vị trí ortho và para:
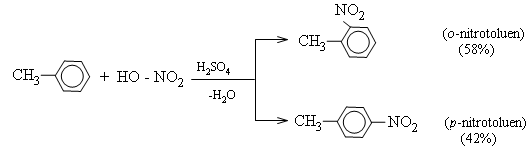
b) Quy tắc thế ở vòng benzen
Khi vòng benzen đã có sắn nhóm ankyl (hay các nhóm –OH, -NH2, -OCH3,...
Phản ứng thế vào vòng sẽ dễ dàng hơn và ưu tiên xảy ra ở vị trí nhóm ortho và para. Ngược lại, nếu ở vòng benzen đã có sẵn nhóm –NO2 (hoặc các nhóm –COOH, -SO3H, ...) phản ứng thế vào vòng sẽ khó hơn và ưu tiên xảy ra ở vị trí meta.
c) Cơ chế phản ứng thế ở vòng benzen
Phân tử halogen hoặc phân tử axit nitric không trực tiếp tấn công. Các tiểu phân mag điện tích dương tạo thành do tác dụng của chúng với xúc tác mới là tác nhân tấn công trực tiếp vào vòng benzen. Thí dụ:
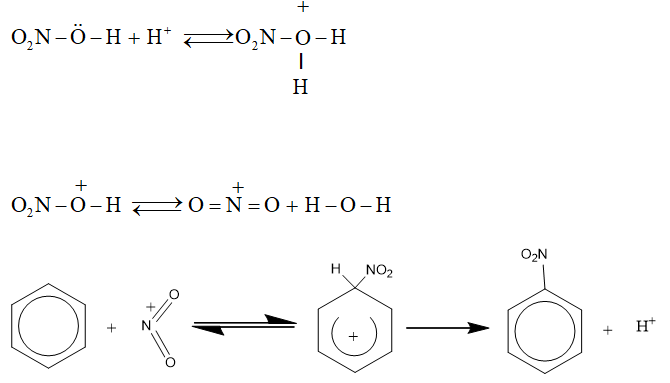
d) Thế nguyên tử H của mạch nhánh
- Do các đồng đẳng của benzen còn có nhánh ankyl nên trong điều kiện thích hợp có thể thế H của nhánh ankyl.
C6H5CH3 + Cl2 → C6H5CH2Cl + HCl (điều kiện ánh sáng và tỉ lệ 1:1)
2. Phản ứng cộng
a) Cộng hiđro
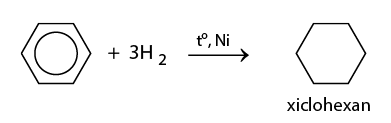
b) Cộng clo
- Dẫn lượng nhỏ khí clo vào bình chứa một ít benzen, đậy kín lại rồi đưa bình ra ngoài ánh nắng. Trong bình xuất hiện khói trắng và thành bình xuất hiện một lớp bột màu trắng. Đó là 1,2,3,4,5,6 - hexacloxiclohexan (hexacloran).
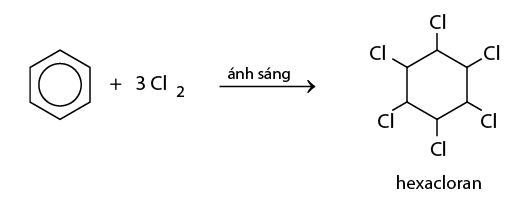
3. Phản ứng oxi hoá
a) Phản ứng oxi hoá không hoàn toàn
Thí nghiệm: Khi đun nóng đồng thời cả hai ống nghiệm trong nồi cách thuỷ:
- Benzen vân không làm mất màu dung dịch kali pemanganat.
- Toluen làm mất màu dung dịch kali pemanganat, tạo kết tủa mangan đioxit.
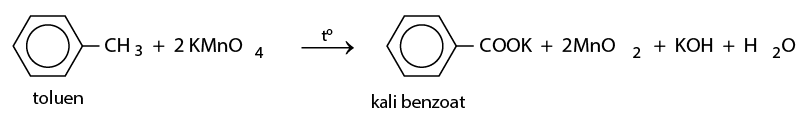
b) Phản ứng oxi hoá hoàn toàn
Các hiđrocacbon thơm khi cháy toả nhiều nhiệt:
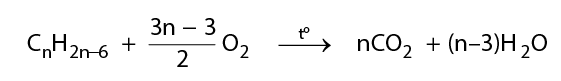
Điều chế
- Benzen thường được tách bằng cách chưng cất dầu mỏ và nhựa than đá. Chúng còn được điều chế từ ankan hoặc xicloankan
CH3[CH2]4CH3 à C6H6 (xt, nhiệt độ, -4H2)
Ứng dụng
- Benzen là nguyên liệu quan trọng nhất của công nghiệp hóa hữu cơ.
- Benzen được dùng nhiều chất để tổng hợp các monome trong sản xuất polime làm chất dẻo, cao su, tơ sợi (chẳng hạn poli stiren, cao su buna – stiren, tơ capron). Từ benzen người ta điều chế ra nitrobenzen, anilin, phenol để dùng tổng hợp phẩm nhuộm, dược phẩm, thuốc trừ dịch hại,...
- Benzen được sử dụng làm dung môi trong công nghiệp và trong phòng thí nghiệm.



