-
Câu Hỏi
1868
-
Thành Viên
799
-
Wiki-Hỏi-Đáp.Org
Wiki Hỏi đáp trực tuyến là website chia sẻ kiến thức cộng đồng về tất cả lĩnh vực từ giáo dục, kinh tế, xã hội khoa học, đời sống, gia đình...
Liên hệ tại: Wikihoidap.org@gmail.com
Liên kết hữu ích bạn nên xem: Alo789
-
Theo dõi Wiki Hỏi đáp
-
Bản quyền tại DMCA
Kali nitrat là muối gì? Cấu tạo, tính chất và cách điều chế
Muối Kali nitrat là muối gì? Tính chất hóa học, đặc điểm, ứng dụng như thế nào trong đời sống? Công thức ra sao? Cùng Wikihoidap.org tìm hiểu nhé!
Danh mục nội dung
KNO3 là chất gì?
Kali nitrat hay còn gọi là diêm tiêu, là hợp chất hóa học có công thức là KNO3. Trong quá khứ, con người đã sử dụng nó để làm một số loại ngòi nổ. Trong tự nhiên chỉ có một lượng nhỏ kali nitrat.
Đây là muối ion của ion kali K+ và ion nitrate NO3-. KNO3 được xem như một tiêu thạch khoáng sản và là một nguồn rắn tự nhiên của nitơ.
Cấu trúc phân tử KNO3
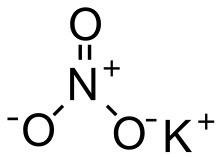
Tính chất vật lý của Kali nitrat
Kali nitrat có cấu trúc tinh thể trực giao ở nhiệt độ phòng, biến đổi thành hệ thống lượng giác ở 129 ° C (264 ° F).
Kali nitrat hòa tan vừa phải trong nước, nhưng độ hòa tan của nó tăng theo nhiệt độ. Dung dịch nước gần như trung tính, thể hiện pH 6,2 ở 14 ° C (57 ° F) cho dung dịch bột thương mại 10%. Nó không hút ẩm lắm, hấp thụ khoảng 0,03% nước trong 80% độ ẩm tương đối trong 50 ngày. Nó không hòa tan trong rượu và không độc hại, nó có thể phản ứng nổ với các chất khử, nhưng bản thân nó không phải là chất nổ.
Đây là muối ít tan trong ethanol nhưng có thể tan trong glycerol, amoni.
Tính chất hóa học của Kali nitrat
KNO3 có tính Oxy hóa rất cao
KNO3 bị nhiệt phân tạo thành kali Nitrít và Oxi với phương trình sau đây:
KNO3 → KNO2 + O2 (Điều kiện xảy ra phản ứng đó là nhiệt độ cao)
Cách điều chế KNO3
Kali nitrat có thể được thực hiện bằng cách kết hợp ammonium nitrate và kali hydroxit .
NH4NO3 (aq) + KOH (aq) → NH3 (g) + KNO3 (aq) + H2O (l)
Một cách khác để sản xuất kali nitrat diêm tiêu mà không có sản phẩm phụ là amoniac là kết hợp amoni nitrat, được tìm thấy trong các túi nước đá, và kali clorua , dễ dàng thu được dưới dạng muối thay thế natri .
NH4NO3 (aq) + KCl (aq) → NH4Cl (aq) + KNO3 (aq)
Kali nitrat cũng có thể được sản xuất bằng cách trung hòa axit nitric với kali hydroxit. Phản ứng này tỏa nhiệt cao.
KOH (aq) + HNO3 → KNO3 (aq) + H2O (l)
Ở quy mô công nghiệp, nó được điều chế bằng phản ứng chuyển vị kép giữa natri nitrat và kali clorua.
NaNO3 (aq) + KCl (aq) → NaCl (aq) + KNO3 (aq)
Ứng dụng trong đời sống
Muối kali nitrat dùng để:
- Chế tạo thuốc nổ đen với công thức: 75% KNO3, 10% S và 15% C. Khi nổ, nó tạo ra muối kali sunfua, khí nitơ và khí CO2:
2KNO3 + S + 3C →to K2S + 3CO2 + N2
- Làm phân bón, cung cấp nguyên tố kali và nito cho cây trồng.
- Bảo quản thực phẩm trong công nghiệp.
- Điều chế oxi với lượng nhỏ trong phòng thí nghiệm bằng phản ứng nhiệt phân.
- Điều chế HNO3 khi tác dụng với axit khó bay hơi:
H2SO4 + 2KNO3 → K2SO4 + 2HNO3
- Phụ gia thực phẩm (E252).
- Kem đánh răng trị ê buốt.



