-
Câu Hỏi
1868
-
Thành Viên
799
-
Wiki-Hỏi-Đáp.Org
Wiki Hỏi đáp trực tuyến là website chia sẻ kiến thức cộng đồng về tất cả lĩnh vực từ giáo dục, kinh tế, xã hội khoa học, đời sống, gia đình...
Liên hệ tại: Wikihoidap.org@gmail.com
Liên kết hữu ích bạn nên xem: Alo789
-
Theo dõi Wiki Hỏi đáp
-
Bản quyền tại DMCA
Định nghĩa năng lượng ion hóa của một nguyên tử hay một phân tử
Mỗi khi học đến phần bảng tuần hoàn, chúng ra lại tiếp cận đến những kiến thức gây khó hiểu như định nghĩa năng lượng ion hóa là gì? Tính chất của năng lượng ion hóa? So sánh năng lượng ion hóa trong bảng tuần hoàn? Cách tính năng lượng ion hóa? Các yếu tố ảnh hưởng đến năng lượng ion hóa?… Cùng tìm hiểu về chủ đề năng lượng ion hóa là gì cùng những nội dung liên quan qua bài viết sau của Wikihoidap.org nhé!
Danh mục nội dung
Định nghĩa năng lượng ion hóa
Năng lượng ion hóa của một nguyên tử hay một phân tử là năng lượng cần thiết để tách một điện tử từ nguyên tử hay phân tử đó ở trạng thái cơ bản. Một cách tổng quát hơn, năng lượng ion hóa thứ n là năng lượng cần thiết để tách điện tử thứ n sau khi đã tách (n-1) điện tử đầu tiên.
Bạn có thể nghĩ về năng lượng ion hóa như một biện pháp của các khó khăn trong việc loại bỏ electron hay sức mạnh mà một electron đang bị ràng buộc. Các năng lượng ion hóa càng cao thì càng khó để loại bỏ một electron. Do đó, năng lượng ion hóa là trong chỉ số về khả năng phản ứng. Năng lượng ion hóa rất quan trọng vì nó có thể được sử dụng để giúp dự đoán sức mạnh của liên kết hóa học.
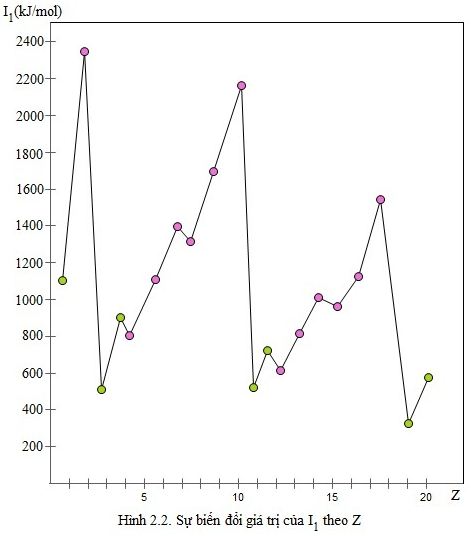
Tính chất của năng lượng ion hóa
Do các e càng xa hạt nhân lực liên kết giữa e và hạt nhân càng nhỏ và ngược lại nên ta có:
Eletron càng gần hạt nhân thì năng lượng ion hóa càng lớn.
Electron càng xa hạt nhân thì năng lượng ion hóa càng nhỏ.
Từ đó suy ra: I1 < I2< …< In
Nguyên tử càng dễ nhường e (tính kim loại càng mạnh) thì I có trị số càng nhỏ.
Công thức tính năng lượng e
+) Năng lượng e trong nguyên tử H:
En = −13,6/n2 (eV) với n ∈ N*: lượng tử số
+) Năng lượng ion hóa nguyên tử H:
ΔE = E∞ − E1 = hc / λ∞1
Lưu ý:
- Năng lượng ion hóa là năng lượng tối thiểu cần thiết để loại bỏ một electron từ một nguyên tử hay ion trong pha khí.
- Các đơn vị phổ biến nhất của năng lượng ion hóa là calo mỗi nốt ruồi (kJ / M) hoặc electronvolt (eV).
- Năng lượng ion hóa thể hiện tính chu kỳ trong bảng tuần hoàn.
- Xu hướng chung là năng lượng ion hóa để tăng di chuyển từ trái sang phải qua một thời gian phần tử. Di chuyển trái sang phải qua một thời gian, bán kính nguyên tử giảm, do đó electron được nhiều thu hút vào (gần) hạt nhân.
- Xu hướng chung là năng lượng ion hóa để giảm di chuyển từ trên xuống dưới xuống một nhóm bảng tuần hoàn. Di chuyển xuống một nhóm, một vỏ hóa trị được bổ sung. Các electron ngoài cùng là thêm từ nhân dươngtính, vì vậy chúng dễ dàng hơn để loại bỏ.
Ví dụ về năng lượng ion hóa
Có hai nguyên tố K, Na. So sánh năng lượng ion hóa thứ nhất của K và Na?
Ta có :
Cấu hình electron của kali: 1s22s22p63s23p64s1
Cấu hình electron của natri: 1s22s22p63s1
K có 6 lớp e, Na có 4 lớp e nên lực liên kết giữa e với hạt nhân của Na lớn hơn của K
=> Năng lượng ion hóa thứ nhất của K < năng lượng ion hóa thứ nhất của Na.



